Gilead meldt doeltreffendheid van 5- en 10-daagse dosering van Remdesivir
Nieuws -> InformatiefBron: Gilead Sciences, Inc.
30-04-2020
Gilead kondigt de resultaten aan van fase 3 van het onderzoek naar Antivirale Remdesivir bij patiënten met een ernstige COVID-19 infectie. Studie toont gelijkaardige doeltreffendheid aan met 5- en 10-daagse dosering van antivirale Remdesivir
FOSTER CITY, Californië - (BUSINESS WIRE) - 29 april 2020 - Gilead Sciences, Inc. (Nasdaq: GILD) kondigde op 29 april 2020 topline resultaten aan van de open-label, Fase 3 SIMPLE proef die de 5-daagse en 10-daagse doseringsduur van de onderzoeksantivirale remdesivir bij gehospitaliseerde patiënten met ernstige manifestaties van COVID-19 ziekte evalueert. De studie toonde aan dat patiënten die een 10-daagse behandelingskuur van remdesivir kregen, een vergelijkbare verbetering van de klinische status bereikten in vergelijking met patiënten die een 5-daagse behandelingskuur volgden (Odds Ratio: 0,75 [95% CI 0,51 - 1,12] op dag 14). Er werden geen nieuwe veiligheidssignalen geïdentificeerd met remdesivir in beide behandelingsgroepen. Gilead is van plan om de volledige gegevens in te dienen voor publicatie in een peer-reviewed tijdschrift in de komende weken.

(Bron Gilead - 2020)
Merdad Parsey, MD, PhD is Gilead's Chief Medical Officer, verantwoordelijk voor het toezicht op de wereldwijde klinische ontwikkeling van het bedrijf en medische zaken organisaties
'In tegenstelling tot de traditionele ontwikkeling van geneesmiddelen proberen we een onderzoeksmiddel te evalueren naast een zich ontwikkelende wereldwijde pandemie. Meerdere gelijktijdige studies helpen ons te weten of remdesivir een veilige en effectieve behandeling is voor COVID-19 en hoe we het middel het beste kunnen gebruiken', aldus Merdad Parsey, MD, PhD, Chief Medical Officer, Gilead Sciences. 'Deze onderzoeksresultaten vormen een aanvulling op de gegevens van de placebogecontroleerde studie van remdesivir, uitgevoerd door het National Institute for Allergy and Infectious Diseases, en helpen om de optimale duur van de behandeling met remdesivir te bepalen. De studie toont het potentieel aan voor sommige patiënten om te worden behandeld met een 5-daagse behandeling, waardoor het aantal patiënten dat met ons huidige aanbod van remdesivir zou kunnen worden behandeld, aanzienlijk zou kunnen toenemen. Dit is vooral belangrijk in het kader van een pandemie, om ziekenhuizen en gezondheidswerkers te helpen meer patiënten te behandelen die dringend zorg nodig hebben.'
Remdesivir is nog nergens ter wereld gelicentieerd of goedgekeurd en het is nog niet aangetoond dat het veilig of effectief is voor de behandeling van COVID-19. In deze studie werd getracht te bepalen of een kortere, 5-daagse kuur van remdesivir vergelijkbare resultaten zou opleveren als het 10-daagse behandelingsschema dat in meerdere lopende onderzoeken naar remdesivir wordt gebruikt. Secundaire doelstellingen waren onder meer het aantal ongewenste voorvallen en aanvullende maatregelen voor de klinische respons in beide behandelingsgroepen. Patiënten moesten bewijs hebben van longontsteking en verminderde zuurstofniveaus die geen mechanische beademing vereisten op het moment van binnenkomst van de studie. Klinische verbetering werd gedefinieerd als een verbetering van twee of meer punten vanaf de basislijn op een vooraf gedefinieerde zevenpuntsschaal, variërend van ziekenhuisontslag tot verhoging van het zuurstofgehalte tot de dood. Patiënten bereikten klinisch herstel als ze geen zuurstofondersteuning en medische zorg meer nodig hadden of uit het ziekenhuis werden ontslagen.
(Bron Gilead - 2020)
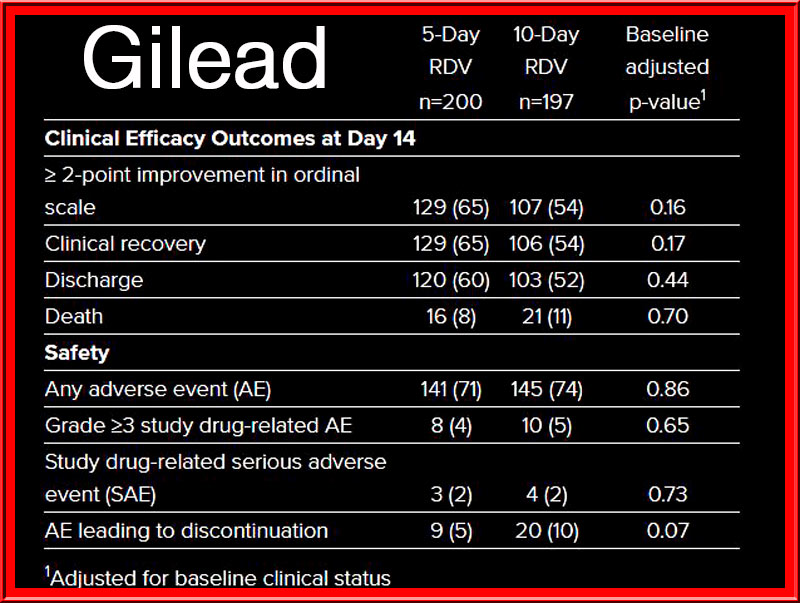
De belangrijkste resultaten van het onderzoek Remdesivir op het gebied van efficiëntie en veiligheid
In deze studie was de tijd tot klinische verbetering voor 50 procent van de patiënten 10 dagen in de 5-daagse behandelgroep en 11 dagen in de 10-daagse behandelgroep. Meer dan de helft van de patiënten in beide behandelingsgroepen werd op dag 14 uit het ziekenhuis ontslagen (5-dagen: 60,0%, n=120/200 vs.10-dagen: 52,3% n=103/197; p=0,14). Op dag 14 bereikte 64,5 procent (n=129/200) van de patiënten in de 5-daagse behandelgroep en 53,8 procent (n=106/197) van de patiënten in de 10-daagse behandelgroep een klinisch herstel.
De klinische resultaten varieerden per geografie. Buiten Italië bedroeg het totale sterftecijfer op dag 14 7 procent (n=23/320) in beide behandelingsgroepen, waarbij 64 procent (n=205/320) van de patiënten een klinische verbetering liet zien op dag 14 en 61 procent (n=196/320) van de patiënten die uit het ziekenhuis werden ontslagen.
Over Remdesivir. Remdesivir is een onderzoeksnucleotide analoog met breed-spectrum antivirale activiteit zowel in vitro als in vivo in diermodellen tegen meerdere opkomende virale pathogenen, waaronder Ebola, Marburg, MERS en SARS. In-vitrotests uitgevoerd door Gilead hebben aangetoond dat remdesivir actief is tegen het virus dat COVID-19 veroorzaakt. De veiligheid en doeltreffendheid van remdesivir voor de behandeling van COVID-19 worden geëvalueerd in meerdere lopende Fase 3 klinische studies.
Over Gilead Sciences. Gilead Sciences, Inc. is een op onderzoek gebaseerd biofarmaceutisch bedrijf dat innovatieve geneesmiddelen ontdekt, ontwikkelt en commercialiseert in gebieden met een onvervulde medische behoefte. Het bedrijf streeft ernaar de zorg voor mensen met levensbedreigende ziekten over de hele wereld te transformeren en te vereenvoudigen. Gilead heeft vestigingen in meer dan 35 landen wereldwijd, met het hoofdkantoor in Foster City, Californië. Voor meer informatie over de reactie van Gilead op de uitbraak van het coronavirus kunt u terecht op de speciale pagina van het bedrijf: https://www.gilead.com/purpose/advancing-global-health/covid-19 .









